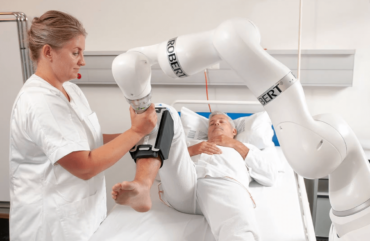
Réussir ses certifications grâce aux normes IEC 60601 et IEC 62366
29 octobre 2022Marquage CE, réussir sa certification, un enjeu majeur pour les dispositifs médicaux.

Marquage CE, un enjeu majeur pour commercialiser votre dispositif médical en Europe
Le respect des contraintes normatives est indispensable pour réussir ses certifications avant mise sur le marché. Ceci est particulièrement complexe pour les fabricants de dispositifs médicaux, soumis à une réglementation très stricte. Cet enjeu majeur s’intègre ainsi dans le processus de conception mis en œuvre par Blanc Tailleur Design R&D.
Notre expérience des normes et certifications médicales constitue notamment un atout précieux pour l’obtention du marquage CE, sésame issu des essais cliniques permettant la commercialisation de vos équipements médicaux.
La prise en compte des Normes au cœur de nos conceptions
Spécialiste de l’innovation produits et des interfaces, par l’usage et la technologie, Blanc Tailleur Design R&D possède une forte expérience des univers techniques et des normes associées.
L’expertise de notre agence de design industriel et de R&D concerne plus particulièrement les dispositifs médicaux, le transport/aéronautique, et les produits à forte complexité technologique.
Nos solutions physiques ou digitales sont le fruit d’un processus de conception itératif tenant compte des trois éléments centraux suivants :
- les besoins utilisateurs à travers l’UX Design (de l’anglais « User eXperience », expérience utilisateur) ;
- les enjeux techniques et normatifs ;
- les aspects marketing et de valorisation de la marque grâce au Design Langage (/design language).
Un levier indispensable pour réussir vos certifications
“ Notre expérience des normes nous permet d’anticiper les essais de certification et donc de réduire les risques de non-conformité. Vous évitez ainsi la mise en place d’actions correctives impliquant des coûts supplémentaires et un allongement des délais de commercialisation. C’est pour nos clients l’assurance d’optimiser coûts et délais.”
Edouard Bert – Gérant et Ludwig Katchynsky – Design manager.
La prise en compte précoce des exigences légales et réglementaires accélère le processus de certification et par conséquent la mise sur le marché. Cette optimisation du time-to-market est capitale pour la réussite de votre projet, notamment dans le médical, un secteur d’activité très cadré et concurrentiel.
Notre expérience des normes relatives aux dispositifs médicaux
Avant de pouvoir être commercialisé dans l’Union européenne, tout dispositif médical doit obtenir le marquage CE.
Pour cela, le produit doit répondre aux exigences réglementaires en matière de santé et sécurité, notamment détaillées dans les normes médicales IEC 60601 et IEC 62366.
Normes médicales IEC 60601
La conformité aux normes IEC 60601 est nécessaire pour la certification des équipements électro-médicaux en Europe et dans de nombreux pays du monde.
Publié par la Commission électrotechnique internationale (International Electrotechnical Commission ou IEC en anglais), cet ensemble de normes comprend :
- des normes générales communes à tous les dispositifs électro-médicaux ;
- des normes collatérales qui complètent les spécifications techniques générales : compatibilité électromagnétique (CEM), radioprotection pour les appareils émettant des rayons X, etc. ;
- des normes particulières qui modifient, annulent ou remplacent les normes générales pour certaines catégories d’équipements : scanners IRM, électro-encéphalographes, etc.
Les dispositifs électro-médicauxLes équipements électro-médicaux sont définis comme des appareils électriques qui :
Exemples : robots chirurgicaux, respirateur, défibrillateurs cardiaques, moniteurs patients, lasers médicaux, matériel d’échographie, etc. |
Norme Usability IEC 62366
La norme IEC 62366 concerne l’utilisabilité (en anglais usability) ou l’aptitude à l’utilisation. En effet, les interactions des usagers avec les dispositifs médicaux à travers une interface utilisateur peuvent induire certaines erreurs.
La norme Usability vise ainsi à identifier, évaluer et réduire les risques associés à une utilisation normale du dispositif médical, et notamment:
- les erreurs de perception (exemple : voyant lumineux ou alarme non remarqué·e) ;
- les erreurs de compréhension (exemple : interprétation erronée de la valeur numérique affichée) ;
- les erreurs de manipulation (exemple : commande mal actionnée).
Les risques liés à un mauvais usage délibéré de l’appareil ne sont pas pris en compte. L’objectif est de concevoir des équipements médicaux sûrs, ergonomiques et intuitifs pour tous l’ensemble des utilisateurs.
L’Ingénierie de l’Aptitude à l’Utilisation (IAU)L’IAU concerne trois aspects du développement d’un dispositif médical :
|
Un atout précieux pour l’obtention de la certification CE
Notre maîtrise des normes médicales IEC 60601 et Usability IEC 62366 contribue à la réussite de vos projets dans le domaine médical. Grâce à notre méthodologie, nous arrivons rapidement à un concept innovant conciliant le besoin d’usage et les contraintes normatives pour obtenir la certification européenne. Vous pouvez ainsi accélérer le processus de marquage CE et sécuriser les délais de commercialisation de votre produit.
Nous avons par exemple livré avec cette approche le prototype du robot chirurgical ROSA, dédié aux opérations du crâne et du rachis. L’ergonomie et la conception mécanique étaient pilotés par l’usage, la norme et la faisabilité. Le robot a ensuite pu être rapidement certifié CE puis commercialisé dans la foulée.
Vous développez un projet innovant pour le marché de la robotique chirurgicale ou le domaine médical ?
Credits photos : @blanc tailleur design R&D